药品企业注册管理办法是国家药品监督管理局为了规范药品注册行为,加强药品监督管理而制定的法规。以下是药品企业注册管理办法的一些主要内容。
1、适用范围:适用于中华人民共和国境内申请药品注册以及药品注册审批相关活动。
2、监管部门:国家药品监督管理部门主管全国药品注册管理工作,负责药品注册的监督实施。

3、注册分类与要求:药品注册分为新药申请、仿制药申请、进口药品申请等类别,每种申请有其特定的要求和流程,申请人需按照相关规定提交相关材料,包括药物的临床前研究、生产工艺、质量控制等。
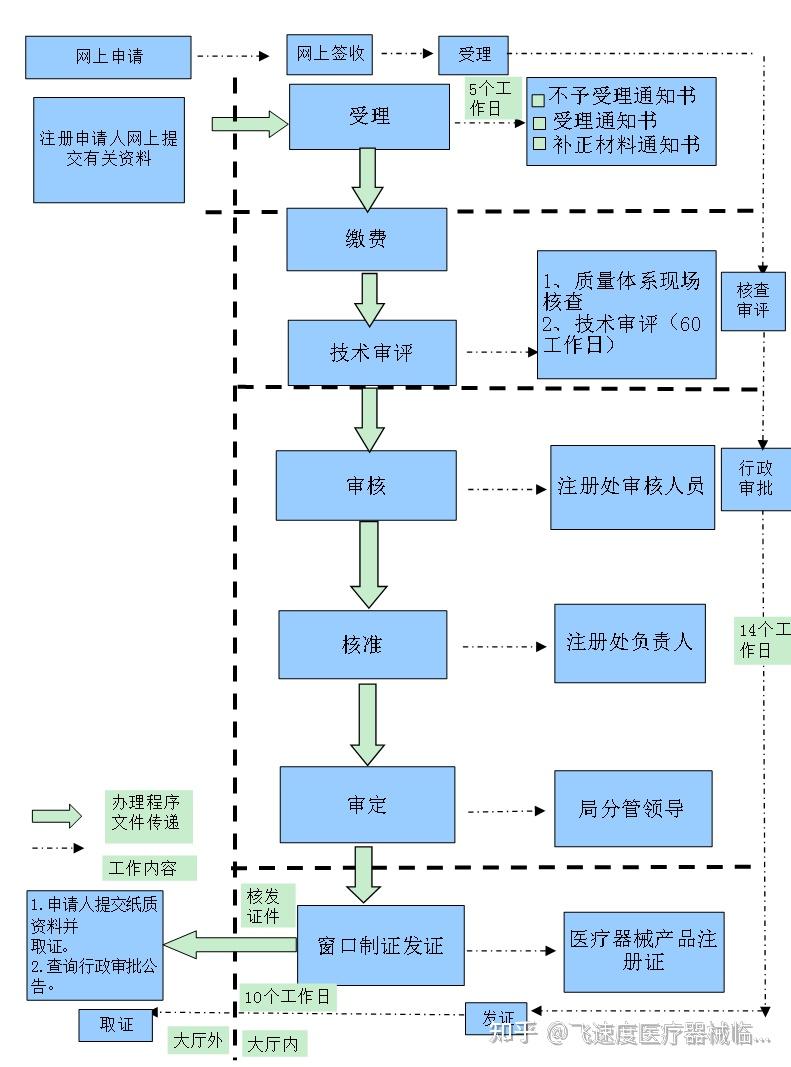
4、审批流程:药品注册审批流程包括形式审查、技术审查、现场核查等阶段,申请人需配合监管部门进行现场核查,确保药品研发、生产和质量的合规性。
5、监督管理:药品监管部门对药品注册申请进行监督管理,对违规行为进行处罚,包括撤销药品批准证明文件、责令停产等,监管部门还负责对已上市药品进行监测和管理,确保药品的安全性和有效性。

6、法律责任:申请人应诚实守信,承担相应法律责任,对于提供虚假材料或隐瞒真实情况的申请人,监管部门将依法追究其法律责任。
仅供参考,如需了解更详细的药品企业注册管理办法,建议查询国家药品监督管理局官网或相关政府部门官网。